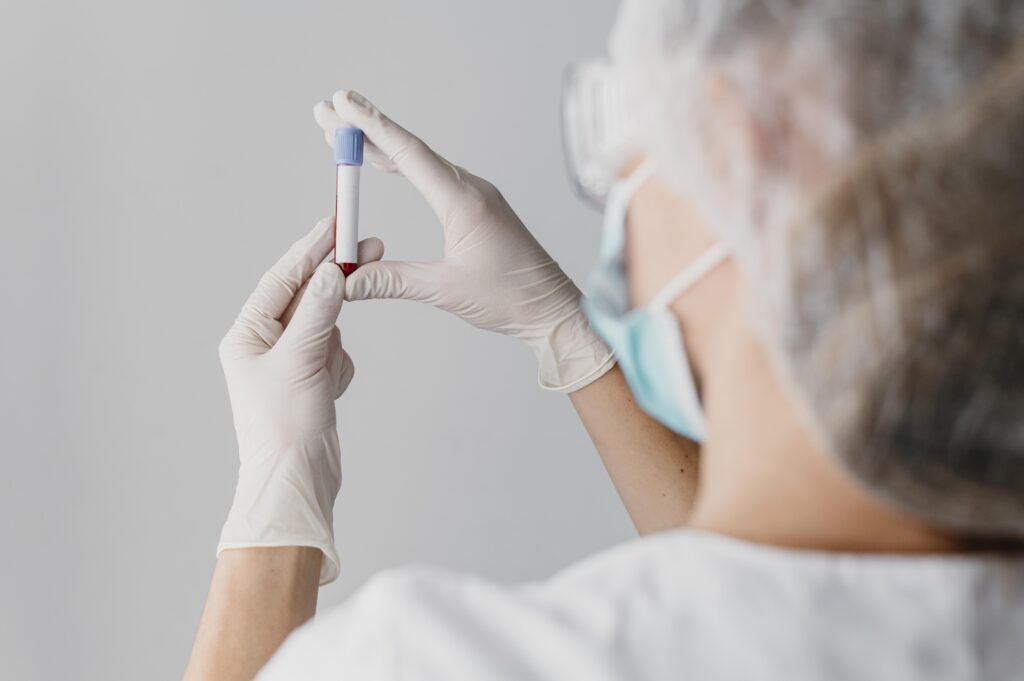
Por décadas, acompanhar a evolução de um tumor significava submeter pacientes a biópsias invasivas e exames de imagem que só mostravam o problema quando já era visível. Uma tecnologia está mudando radicalmente esse cenário: a biópsia líquida. Este exame de sangue é capaz de detectar fragmentos de DNA liberados por células tumorais, abrindo uma janela em tempo real para o comportamento do câncer e permitindo monitorar a resposta ao tratamento com uma precisão antes inimaginável .
O que é biópsia líquida e o que ela detecta?
Diferentemente da biópsia convencional, que retira um fragmento do tumor por cirurgia ou punção, a biópsia líquida analisa uma simples amostra de sangue em busca de biomarcadores liberados pelas células cancerígenas. O principal deles é o DNA tumoral circulante (ctDNA) – fragmentos de material genético que as células tumorais liberam na corrente sanguínea durante seu crescimento e morte .
A grande inovação está no fato de que o ctDNA carrega as mesmas mutações genéticas presentes no tumor de origem. Ao sequenciar esse material, os médicos podem identificar alterações moleculares que orientam o uso de terapias-alvo, sem necessidade de nova biópsia tecidual. E mais: como o tumor é geneticamente heterogêneo, uma única biópsia líquida pode capturar mutações de diferentes metástases que talvez não fossem representadas em um fragmento de tecido isolado .
O poder preditivo: Antecipando a resposta ao tratamento
Um estudo conduzido pelo Instituto de Pesquisa do Câncer de Londres (ICR), publicado em 2026, demonstrou que a medição dos níveis de ctDNA antes mesmo do início do tratamento e após apenas quatro semanas pode prever com impressionante precisão se o paciente responderá à terapia .
No estudo, 167 pacientes com câncer de mama avançado foram divididos com base no perfil molecular de seus tumores. Aqueles com níveis mais baixos de ctDNA antes do tratamento tiveram sobrevida livre de progressão significativamente maior. Entre as pacientes com câncer de mama triplo negativo, as que apresentavam baixo ctDNA inicial viveram 10,2 meses sem progressão, contra apenas 4,4 meses daquelas com níveis elevados .
Após quatro semanas de tratamento, pacientes cujo ctDNA se tornou indetectável tiveram o câncer controlado por 12 meses, enquanto aquelas que ainda apresentavam ctDNA detectável regressaram em apenas 4,3 meses. A diferença na taxa de resposta foi gritante: 85,7% contra 11,4%. Como explicou Iseult Browne, primeira autora do estudo, “saber disso logo no início significa que podemos evitar administrar medicamentos que não funcionarão e oferecer alternativas antes que o câncer tenha a chance de crescer” .
Detecção precoce de resistência e o cenário brasileiro
A aplicação mais revolucionária da biópsia líquida é identificar mutações de resistência muito antes de qualquer evidência clínica de progressão. O exemplo clássico ocorre no câncer de pulmão com mutações no gene EGFR. Pacientes que respondem bem aos inibidores podem adquirir a mutação T790M, que confere resistência. Um estudo conduzido no Hospital de Amor, em Barretos (SP), demonstrou a viabilidade de detectar essa mutação por biópsia líquida em pacientes brasileiros, permitindo a troca precoce para medicamentos de nova geração .
Um dos achados mais notável ocorreu em um participante assintomático de um programa de rastreamento: a biópsia líquida detectou uma mutação no gene TP53 seis meses antes do diagnóstico de câncer de pulmão, demonstrando seu potencial para detecção precoce em populações de risco .
Na prática clínica brasileira, a técnica ainda enfrenta barreiras. O teste custa cerca de R$ 6 mil por paciente, valor proibitivo para a maioria. No SUS, o acesso é restrito a poucos centros de referência. No entanto, o estudo brasileiro trouxe uma vantagem logística importante: demonstrou que o painel utilizado detecta ctDNA mesmo em amostras congeladas, sem necessidade de tubos especiais, ampliando a possibilidade de adoção em serviços públicos .
Limitações e o futuro da oncologia de precisão
Apesar do entusiasmo, a biópsia líquida não substitui completamente a biópsia tecidual. Em estágios iniciais, a quantidade de ctDNA pode ser muito baixa para detecção confiável. Um resultado negativo não exclui a presença de mutações, sendo necessária a confirmação com tecido sempre que possível .
Além disso, nem todos os tumores liberam quantidades detectáveis de material genético. A sensibilidade varia conforme o tipo, estágio e localização do câncer. Por isso, diretrizes internacionais recomendam a biópsia líquida em situações específicas: quando a biópsia convencional não é viável, apresenta risco elevado, ou para monitorar a emergência de resistência ao longo do tratamento .
Ainda assim, a biópsia líquida representa uma mudança de paradigma. Pela primeira vez, médicos podem acompanhar a evolução genética de um tumor em tempo real, ajustando terapias antes que a resistência se consolide. Como resume Nicholas Turner, pesquisador do ICR, “isso tem o potencial de tornar as decisões de tratamento mais rápidas, mais personalizadas e, em última análise, mais eficazes”.
Referências bibliográficas:
Ferro Leal, L., et al. (2025). Feasibility of a ctDNA multigenic panel for non-small-cell lung cancer early detection and disease surveillance. Molecular Oncology. Publicado em 10 de outubro de 2025.
Browne, I. M., Turner, N. C., Chandarlapaty, S., et al. (2026). The Prognostic and Predictive Impact of ctDNA Levels in Patients with Advanced Breast Cancer Enrolled on the plasmaMATCH Trial. Clinical Cancer Research, 32(1), 148-158.
Nota editorial: ferramentas de inteligência artificial foram utilizadas como apoio na redação preliminar. O conteúdo final passou por revisão crítica, ajustes conceituais e validação humana.
Leia outros textos do nosso site:
A genética da cor em animais
Gostou? Compartilhe!



Deixe um comentário